国内电生理渗透率更低,处于快速发展阶段。尽管国内过速性心律失常患者人数庞大,但受限于相关疾病早筛尚未推广、电生理手术难 度高等因素,电生理治疗渗透率仍...
2024-03-08 8 医药医疗器械行业报告
TAA 大量在于肿瘤细胞膜表面,较少正常组织中表达。不同 TAA 可以作为 Car-T 细胞的靶抗原,对 Car-T 起定向作用。靶抗原的选择对于 Car 的特异性、有效性 以及基因改造 T 细胞自身的安全性等都是关键的决定因素。因此,选择合适的靶 点蛋白,是 Car-T 细胞免疫治疗在肿瘤临床研究应用中的一个重要挑战。CD 分 子表达作为表面标志物可用于细胞类型鉴定,以 CD19 为靶点的 Car-T 细胞的临 床研究是目前各国 Car-T 研究中最热门的靶点。除了 CD19 这个被广泛报道的靶 点外,许多肿瘤相关靶点已进入 I 期和 II 期临床试验。Car-T疗法最早由Gross等于上世纪80年末提出,至今已有30余年的发展历程, 是目前过继性 T 细胞治疗中发展最为成熟的技术之一,FDA 在 2017 年批准了首 个 CAR-T 细胞治疗产品,更是正式宣告了 Car-T 技术的产业化成熟。
2017 年的 8 月 30 日,人类抗癌历史上发生了一个值得铭记的大事件,在这天美 国食品和药物管理局(FDA)批准诺华公司的突破性 CAR-T 免疫疗法 Kymriah,成 为全球第一个获批的 CAR-T 细胞治疗产品,用于治疗难治性,或出现二次及以上 复发的 25 岁以下的 B 细胞急性淋巴细胞白血病患者,定价 47.5 万美元。 在 FDA 发布的批文的开头,写着这样一句话:“今天,美国 FDA 做了一个历史性 的决定,在美国境内批准了第一个基因治疗产品,给癌症等其他严重威胁生命的 疾病开辟了全新的治疗途径。” 2017 年 10 月 18 日,Kite Pharma 的 CAR-T 产品 YesCarta(axicabtagene ciloleucel,KTE-C19)经美国 FDA 批准上市,用于治疗成人复发或难治性大 B 细胞淋巴瘤。YesCarta 是全球第二款获批上市的 CAR-T 产品,同时也是第一个 用于治疗非霍奇金淋巴瘤的 CAR-T 产品。 两款 Car-T 产品的获批,给本就已经火热的免疫治疗市场又注射了一剂强心剂。 尽管获批的两款二代 Car-T 仍有许多不足之处,但其产品本身令人瞠目的疗效, 令市场为之疯狂。
第一代 CAR 的组织结构:(A)编码 ScFv 片段的第一代 CAR 的嵌合基因序列、可 识别肿瘤相关抗原的抗原结合区、铰链、跨膜结构域(TM)和信号域,例如 CD3 ζ。第一代 CARs 没有共刺激分子,但包含细胞内信号域。(B)第一代嵌合 CAR 在 T 细胞中的表达。使用各种基因转染方法在 T 细胞中表达嵌合基因序列。T 细 胞中的嵌合基因序列通过蛋白质翻译后表达不干扰内源性 T 细胞受体的功能齐 全的 CAR。(C)在 T 细胞中表达时,第一代 CAR 可变区的放大视图。 1993 年,第一代基于 CD3-ζ链的 CAR-T 细胞被发展出来。该 CAR-T 细胞虽然具 有激活 T 细胞的特点,但是只含有激活受体 CD3-ζ,其抗肿瘤效果比较弱,在 体内的持续扩增有限,不具备大规模杀灭肿瘤细胞的能力。

标签: 医药医疗器械行业报告
相关文章
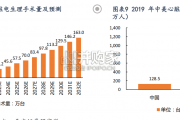
国内电生理渗透率更低,处于快速发展阶段。尽管国内过速性心律失常患者人数庞大,但受限于相关疾病早筛尚未推广、电生理手术难 度高等因素,电生理治疗渗透率仍...
2024-03-08 8 医药医疗器械行业报告
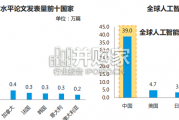
近年来,国内关于人工智能领域的研究十分密集,发文量激增。目前,中国不论在高水平论文还是专利申请数量上都位居世界前列,视觉、语 音、自然语言处理等基础智...
2024-03-07 26 医药医疗器械行业报告

RSV疫苗上市后表现亮眼。据GSK的财报,AREXVY上市后首个季度2023Q3的销售额达7.09亿英镑(约8.5亿美元)全年销售额达12.38亿英镑...
2024-03-05 22 医药医疗器械行业报告
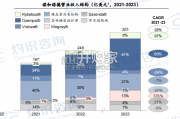
口服胰岛素可更好地模拟人体内胰岛素自然 生理分泌。 正常情况下,胰岛素由胰岛 β 细胞分泌, 经门静脉直接进入肝脏,人体分泌的胰 岛素80%进入肝脏与...
2024-03-04 29 医药医疗器械行业报告
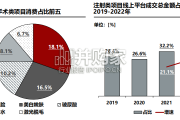
根据2022年新氧医美行业白皮书,2022年非手术类项目消费占比前五的分别是除皱瘦脸、美白嫩肤、玻尿酸、保湿补水和激光脱毛,其中除皱瘦脸和美白嫩肤项目...
2024-03-03 41 医药医疗器械行业报告
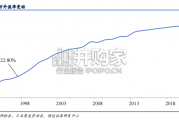
1978 年前,我国医院的所有投资和开销都来自于政府财政,医院主要专注于医疗服务。1978 年改革开放后,国 家财政拨款仅提供医院开支的 10%左右,...
2024-03-02 39 医药医疗器械行业报告
最新留言