国内电生理渗透率更低,处于快速发展阶段。尽管国内过速性心律失常患者人数庞大,但受限于相关疾病早筛尚未推广、电生理手术难 度高等因素,电生理治疗渗透率仍...
2024-03-08 17 医药医疗器械行业报告
粒细胞集落刺激因子(G-CSF)是国内外临床指南首推的用于放化疗相关中性粒细胞减少症治疗药物,包括 短效和长效两种类型。短效G-CSF在每个化疗周期内需要每日给药1~2次,长效G-CSF主要通过聚乙二醇修 饰来制备,在一个化疗周期中往往只需给药1次。预防乳腺癌化疗后中性粒细胞减少的多中心、随机、对照、III期临床研究 ✓ 研究表明:硫培非格司亭非劣效甚至优于短效rhG-CSF,3度以上ANC减少的持续时间:硫培非格司亭两组 优于rhG-CSF(1.06、1.23 vs 2.06天)。固定剂量应用方便效果佳;多周期应用有更好的获益,第2-4周期 3度以上栗缺发生率进一步下降。具有很好的安全性,最常见不良反应为疼痛(约12.6%)和血红蛋白下降 (约12.6%)。 恒瑞医药的硫培非格司亭于2018年5月获批,2019年4月起主动在辽宁、安徽、江苏等省份降价(6800元/ 支降为3680元/支)。2018年度销售额约为1.5亿元,2019H1销售达成约1.4亿元,石药/齐鲁/恒瑞价格分 别为1690元/1705元/1840元(折成3mg/支)。
特瑞普利单抗是首个国产以PD-1为靶点的单抗药物,于2018年12月获批上市,适应症为治疗既往标准治疗 失败后的局部进展或转移性黑色素瘤。拓益自2016年初开始临床研发,至今已在中、美等多国开展了覆盖 14个瘤种的30多项临床研究,积极探索本品在鼻咽癌、尿路上皮癌、肺癌、胃癌、食管癌、肝癌、乳腺癌等 适应证的疗效。 特瑞普利单抗用于标准治疗失败后的晚期尿路上皮癌的II期临床研究(POLARIS-03研究)。研究表明:截至2019年9月5日,在106例可评估患者中,特瑞普利单抗总体人群的客观缓解率(ORR)为 26.4%,疾病控制率(DCR)为50.9%,平均起效时间为9.03周。其中,PD-L1表达阳性患者免疫治疗有效率 高达42.4%,是目前国内外PD-1/PD-L1单药治疗公开数据中最高的。
KN046是康宁杰瑞公司开发的新一代PD-L1/CTLA-4双特异性阻断剂,KN046与PD-L1的亲和力是CTLA-4 的24倍,与CTLA-4的结合部位比Ipilimumab更安全,具有PD-1/PD-L1阻断、CTLA-4阻断和完整Fc段功能 ,在体外实验中KN046对IL2的释放活性为PD-L1单抗和CTLA-4单抗联合的10倍。2018年6月在澳洲启动首 个I期临床研究,预计2021年报产。 KN046在中国晚期实体瘤受试者中的安全性、耐受性、药代动力学以及抗肿瘤活性的初步数据总结。 研究结果表明:ORR为12.2%,DCR为67.3%。KN046在晚期实体瘤患者、尤其是鼻咽癌患者中观察到良好 的抗肿瘤活性,超过50%患者持久临床获益。另外,KNO46人体安全性/耐受性良好,未观察到长期给药毒 性。2019年4月针对晚期NSCLC适应症的II期临床研究启动,计划入组149人,于全国10-15家中心进行。

标签: 医药医疗器械行业报告
相关文章
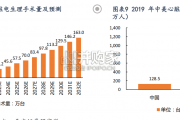
国内电生理渗透率更低,处于快速发展阶段。尽管国内过速性心律失常患者人数庞大,但受限于相关疾病早筛尚未推广、电生理手术难 度高等因素,电生理治疗渗透率仍...
2024-03-08 17 医药医疗器械行业报告
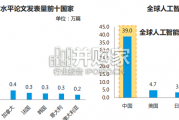
近年来,国内关于人工智能领域的研究十分密集,发文量激增。目前,中国不论在高水平论文还是专利申请数量上都位居世界前列,视觉、语 音、自然语言处理等基础智...
2024-03-07 31 医药医疗器械行业报告

RSV疫苗上市后表现亮眼。据GSK的财报,AREXVY上市后首个季度2023Q3的销售额达7.09亿英镑(约8.5亿美元)全年销售额达12.38亿英镑...
2024-03-05 22 医药医疗器械行业报告
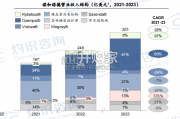
口服胰岛素可更好地模拟人体内胰岛素自然 生理分泌。 正常情况下,胰岛素由胰岛 β 细胞分泌, 经门静脉直接进入肝脏,人体分泌的胰 岛素80%进入肝脏与...
2024-03-04 30 医药医疗器械行业报告
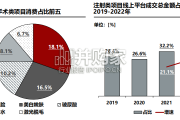
根据2022年新氧医美行业白皮书,2022年非手术类项目消费占比前五的分别是除皱瘦脸、美白嫩肤、玻尿酸、保湿补水和激光脱毛,其中除皱瘦脸和美白嫩肤项目...
2024-03-03 42 医药医疗器械行业报告
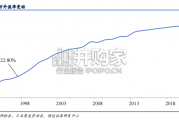
1978 年前,我国医院的所有投资和开销都来自于政府财政,医院主要专注于医疗服务。1978 年改革开放后,国 家财政拨款仅提供医院开支的 10%左右,...
2024-03-02 39 医药医疗器械行业报告
最新留言